Prav možno je, da bi besedna zveza “genetska cepiva” še nedavno povzročila pravo nevihto protestov in zgražanja zagovornikov “naravnega” pristopa k življenjskemu slogu, zdravju in prehranjevanju. Združuje namreč pojma cepljenje in genska tehnologija, kar vsaj v krogih privržencev vsega naravnega niso ravno besede, ki sprožajo odobravanje. A pandemija novega koronavirusa je tovrstne hitre čustvene odzive, ki jih praviloma ne spremlja resen razmislek, marsikje že močno preoblikovala.
Kako telo pripraviti na spopad z virusom?
Cepljenje je metoda, s katero imunski sistem posameznika spodbudimo, da razvije učinkovito obrambo proti bolezni, ne da bi se z boleznijo sploh okužil oziroma jo prebolel. Pri marsikateri bolezni lahko prebolevanje pusti resne posledice na telesu, v določenih primerih pa telo bolezni sploh ne uspe premagati, ker napreduje hitreje, kot se uspe telo pred njo ubraniti, zato se je vsekakor smiselno preventivno zaščititi.
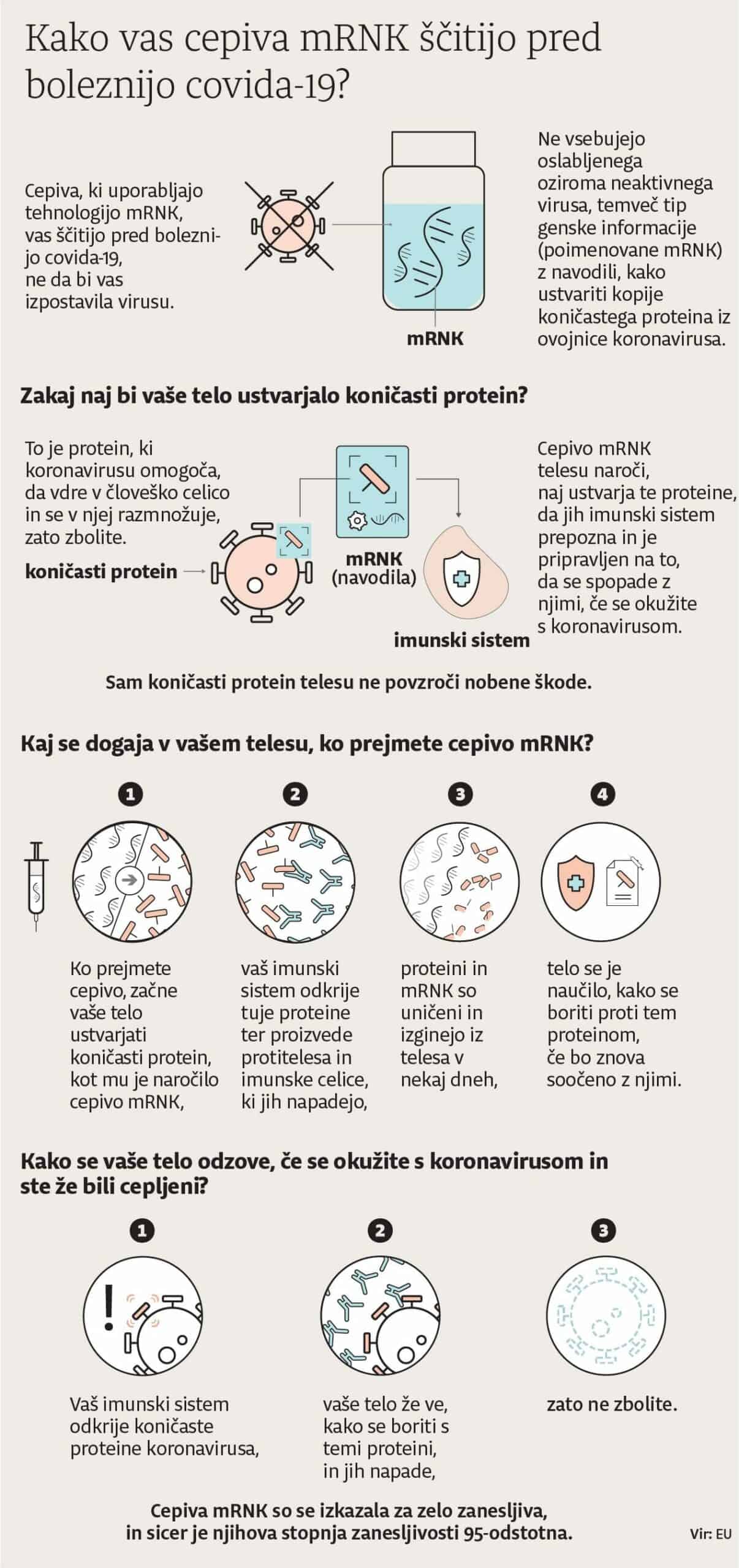
S cepljenjem želimo v telesu vnaprej sprožiti imunski odziv, pri katerem nastanejo posebne molekule in celice, ki so prilagojene za boj prav s točno določenim virusom ali drugim povzročiteljem bolezni, proti kateremu se želimo ubraniti. Pri klasičnih cepivih smo imunski odziv dosegli z vbrizganjem močno oslabljenega virusa ali njegovih značilnih beljakovin, kar je bilo dovolj, da je telo sprožilo izdelavo posebej prilagojenega “orožja”, hkrati pa cepivo ni povzročilo bolezni.
Pri novi tehnologiji genetskega cepiva v tovarni ne izdelajo in nato v telo ne vbrizgajo dejanskih virusnih beljakovin, ampak le informacijo v obliki molekul RNK ali DNK. Ko te molekule prispejo v celice telesa, začnejo izdelovati beljakovine, ki jih nato kot tujke prepozna imunski sistem in izdela posebej prilagojeno orožje za obrambo.
Dolgotrajen razvoj tehnologije genetskih cepiv
Ideja, da bi lahko s pomočjo umetno izdelanih molekul RNK celicam sporočali, katere beljakovine naj proizvajajo in tako zdravili hude bolezni ali metodo uporabili kot obliko cepljenja, je stara že več desetletij. Leta 1990 je skupina raziskovalcev prvič poročala, da jim je v miške uspelo vbrizgali molekule mRNK, v katerih so bili zapisani podatki za izdelavo beljakovine, nato pa so pokazali, da so celice v miškah dejansko začele izdelovati prav to beljakovino.
Čeprav se zdi ideja dokaj preprosta, je bilo treba za učinkovito izvedbo procesa razrešiti še veliko praktičnih težav. Molekule mRNK je mogoče razmeroma hitro izdelati v velikih količinah, zato bi takšna metoda lahko močno poenostavila sicer dolgotrajen klasični postopek proizvodnje cepiva. A molekule mRNK je bilo treba izdelati in zapakirati na način, da so nepoškodovane prispele v celice, hkrati pa je bilo treba preprečiti, da bi molekule sprožile kake druge neželene procese v telesu. Da so razrešili vse te probleme, je trajalo kar dosti časa.
Ključna težava pri razvoju metode je bila, da so molekule mRNK zelo krhke in hitro razpadejo. Najti je bilo treba način, kako jih učvrstiti, da bodo v celicah obstojne vsaj nekaj ur ali dni. Prav tako je bilo treba iznajti učinkovito metodo, kako molekule spraviti v celice. Velik preboj se je zgodil leta 2005, ko je raziskovalcem uspelo molekule mRNK prilagoditi, da so postale bolj stabilne, leta 2015 pa so iznašli še način, kako jih učinkovito zapakirati v majhne lipidne mehurčke. Ključno vlogo pri večini teh odkritij, ki so omogočile nastanek RNK cepiv, je imela madžarska biokemičarka Katalin Karikó, ki je prav zato letos resna kandidatka za Nobelovo nagrado.
Podobno kot RNK cepiva delujejo tudi cepiva, ki imajo genetsko informacijo zapisano v molekuli DNK. Ker so molekule DNK bolj stabilne, jih lahko shranjujemo pri višji temperaturi, nižja pa je tudi cena njihove izdelave. Namesto v lipidne mehurčke molekule DNK vstavijo v ovojnico neškodljivega virusa, ki ima sposobnost, da molekule ob cepljenju prenese v človeške celice, kjer se začnejo na osnovi navodil, ki so zapisana v DNK zaporedju, tvoriti molekule RNK. Od tu naprej poteka vse zelo podobno kot pri RNK cepivih.
Dolgotrajen postopek preizkušanja cepiv
Vsako cepivo mora pred odobritvijo preiti predpisan postopek za preverjanje varnosti in učinkovitosti. Ker denar za boj proti pandemiji tokrat ni bil problem, so lahko študije cepiva za covid-19 izvedli na zelo velikem številu prostovoljcev, kar je dodatno pospešilo postopke.
Poleg varnosti je pri novih genetskih cepivih zelo pomembno tudi, da so se izkazala za izjemno učinkovita. V zelo velikem delu cepljenih preprečijo razvoj simptomov bolezni, pri prav vseh cepljenih, ki so sodelovali v kliničnih študijah, pa so cepiva preprečila hud potek bolezni.
V različnih fazah preskušanja cepiva testirajo predvsem njihovo varnost in učinkovitost. Predklinična faza poteka na živalih, klinične faze pa na ljudeh. V predklinični fazi vbrizgajo cepivo v miške in natančno spremljajo, kako se odzivajo. Raziskovalce zanima, ali razvije ustrezen imunski odgovor in če so po cepljenju dejansko zaščitene pred okužbo.
V prvi fazi klinične študije nato cepivo vbrizgajo manjši skupini zdravih prostovoljcev, pri čemer ponovno preverjajo morebitne stranske učinke in določijo, kakšni sta minimalna in maksimalna doza cepiva.
V drugi fazi poskusijo v testni skupini čim bolje ponazoriti dejansko demografsko strukturo ljudi, ki jim je cepivo namenjeno. Med poskusnimi prejemniki cepiva so tako ljudje vseh generacij, obeh spolov, z različnimi pridruženimi boleznimi in podobno. Tudi v drugi fazi spremljajo morebitne stranske učinke in učinkovitost, predvsem pa želijo ugotoviti ali je izbrana doza cepiva primerna.
Pri tretji fazi gre za preizkus delovanja cepiva v resničnih okoliščinah, saj le polovica udeležencev dobi dejansko učinkovino, druga polovica pa placebo. Po koncu študije preštejejo, kdo med tistimi, ki so zboleli, je dobil cepivo in kdo ne. Na osnovi teh podatkov izračunajo učinkovitost cepiva. Vsa v EU odobrena cepiva so prestala vse faze kliničnih študij in so po mnenju pristojnih agencij povsem varna.
Tehnologija genskih cepiv
Pomembna značilnost nove tehnologije genskih cepiv je, da jih lahko zelo hitro prilagodijo za novi virus oziroma novo bolezen. Če potrebujejo pri cepivu za gripo približno pol leta, da ustrezno oslabljen in prilagojen virus namnožijo v ogromnih količinah kokošjih jajc, je izdelava molekul RNK bistveno hitrejša in bistveno bolj čista.
Tako so v začetku leta 2020 že obstoječe in delujoče platforme za izdelavo cepiva v nekaj dneh oziroma tednih po objavi genoma novega koronavirusa priredili, da so proizvedle prve kandidate za cepivo. V bodoče bo mogoče prav zato cepivo dokaj hitro prilagoditi tudi za nove mutacije oziroma verzije virusa.
Virusi, ki imajo svoj dedni zapis spravljen v molekulah RNK, se namreč spreminjajo pogosteje kot virusi z genomom v obliki molekul DNK. A težavo prestavljajo predvsem mutacije, ki virusu omogočijo lažji prenos okužbe med ljudmi, do česar je med mnogimi mutacijami do sedaj prišlo predvsem pri britanskem in južnoafriškem sevu virusa SARS-CoV-2. Problem predstavljajo tudi mutacije, ki virus na ključnih mestih toliko spremenijo, da jih posebej izdelano “orožje” imunskega sistema, ki ga telo vzpostavi med prebolevanjem bolezni ali ob cepljenju, ne prepozna več.
Tehnologije na osnovi molekul mRNK ne razvijajo le za izdelavo cepiv, ampak tudi za zdravljenje raka in nekaterih drugih hudih bolezni. Čeprav se morda komu zdi, da gre za povsem novo tehnologijo, ki so jo iznašli letos, v resnici tovrstne metode že vrsto let intenzivno preučuje veliko skupin znanstvenikov povsod po svetu. Razvoj nove genske metode za izdelavo cepiv je trajal podobno dolgo kot razvoj starejših klasičnih metod.
Za hiter začetek dobave cepiva proti covid-19 pa ni bila zaslužna le nova tehnologija, ampak tudi odločitev, da se vzporedno s preverjanjem varnosti in učinkovitosti cepiva začne tudi že z množično proizvodnjo. Šlo je za zavestno tveganje, saj bi morali ob neuspešnih testih že izdelano cepivo zavreči. A se je izplačalo. Za hiter razvoj cepiva je bilo, poleg odprtega deljenja informacij in obstoja nove tehnologije, pomembno tudi, da je bilo na voljo veliko javnega denarja.
Primer izvedbe cepljenja v Izraelu
Glede pristopa k izvedbi cepljenja je morda zanimiv primer Izraela, kjer so se cepljenja lotili sistematično in strateško. Najprej so si zagotovili dovolj doz cepiva za vse prebivalce, kar jim je uspelo med drugim zato, ker so s podjetjem Pfizer sklenili dogovor, da bodo med množičnim cepljenjem izvajali dodatne raziskave. Za odmerek cepiva so plačali tudi občutno višjo ceno kot EU.
V Izraelu sedaj poteka množična študija na celotni populaciji države, pri kateri natančno spremljajo vse neželene in želene učinke cepiva in o tem obveščajo tudi proizvajalca cepiva. Za varovanje osebnih podatkov je menda ustrezno poskrbljeno. Raziskovalce zanima predvsem, kako hitro cepljeni pridobijo protitelesa po različnih skupinah in glede na starost, spol, predhodne bolezni ipd.
Pri ministrstvu za zdravje so vzpostavili tudi posebno krizno skupino zdravnikov in strokovnjakov za komuniciranje, ki spremlja morebitne pomisleke med posameznimi družbenimi skupinami in se nanje sistematično odziva.
Težave so imeli denimo z ortodoksnimi religioznimi skupinami in manjšinami, a so pomisleke proti cepljenju uspešno naslovili s pomočjo vidnih predstavnikov teh skupin, ki jim ljudje zaupajo. Sedaj, ko je precepljenost že razmeroma velika, se je med ljudmi začel širiti strah pred tem, da jih bodo morda pozabili cepiti, ne da bi bili v cepljenje prisiljeni.